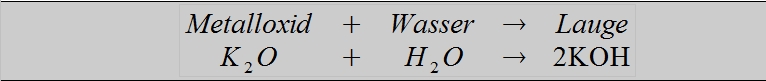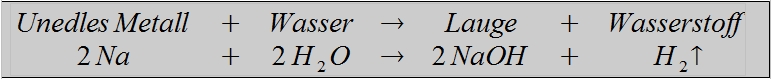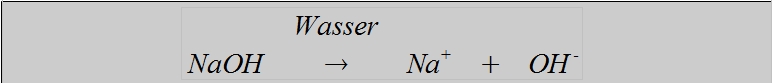Was sind Laugen? Bildung, Eigenschaften & Beispielexperimente
Was sind Laugen?
Ein anderer Begriff für das Wort Lauge ist alkalische Lösung. Damit sind Laugen streng genommen nichts anderes als wässrige Lösungen von Alkalihydroxiden/Metallhydroxiden wie:
- Lithiumhydroxid (LiOH)
- Natriumhydroxid (NaOH)
- Kaliumhydroxid (KOH)
- Rubidiumhydroxid (RbOH)
- Caesiumhydroxid (CsOH)
Wie man an den Verhältnisformeln der aufgeführten Alkalihydroxiden erkennen kann, setzen sich diese aus Alkalimetall-Ionen und Hydroxidionen (OH) zusammen.
Im weiteren Sinne versteht man unter dem Begriff „alkalische Lösung“ auch jede Lösung von Basen.
Im Umkehrschluss erhält man die oben genannten Metallhydroxide, indem man die Laugen eindampft.
Kalilauge
Die Kalilauge ist die wässrige Lösung des Kaliumhydroxids (auch Ätzkali genannt) KOH:
KOH –Wasser-> K+ + OH–
Wie die Natronlauge, ist auch die Kalilauge eine sehr starke Lösung. Das Kaliumhydroxid besitzt ähnliche Eigenschaften wie Natriumhydroxid.
Verwendung der Kalilauge
- Zur Herstellung von Schmierseife
- Für die Gewinnung von andere Kaliumsalze
- Für die Verwendung bei Farbstoffsynthese
- Als Abbeizmittel
- Früher wurde Kalilauge für die Entwicklung von Filmen benötigt
Im Labor lässt sich mit Kalilauge auch Kohlenstoffdioxid aus Gasgemischen entfernen. Dies ist möglich, da es mit dem gelösten Kaliumhydroxid zu Kaliumcarbonat reagiert:
2KOH(aq) + CO2 -> K2CO3+H2O(l)
Natronlauge
Unter dem Begriff Natronlauge versteht man die wässrige Lösung des Natriumhydroxids NaOH:
NaOH –Wasser-> Na+ + OH–
Die Natronlauge zählt sich zu den stärksten Laugen. Sie weicht tierische und pflanzliche Stoffe erst auf und löst sie anschließend. Deshalb findet man Natronlauge im Alltag oft in Putzmitteln wie Geschirrspülmittel, Rohrfrei Reinigern, aber auch in Lebensmitteln, wie der Laugenbrezel, ist Natronlauge enthalten.
Verwendung der Natronlauge
- Zur Herstellung von Seife
- Als Lebensmittelzusatzstoff bei Laugengebäck
- Zum Reinigen von Flaschen in Getränken-Abfüllanlagen
- Zum Entfernen von alter Farbe
- Zur Veredelung von Baumwolle (Merzerisation)
- Zum Entfernen von Erdöl- und Fettrückstände
- Zur Neutralisation von Säuren (z.B. in Abwasseraufbereitung und der Behandlung von Trinkwasser)
- Als Bestandteil von Reinigungsmittel z.B. Rohrreinigung
- Zur Analyse von Wein (z.B. zur Bestimmung von Acetaldehyd in süßen Wein)
Kalkwasser
Kalkwasser ist die Bezeichnung für die wässrige Lösung des Calciumhydroxids (auch gelöschter Kalk genannt) Ca(OH)2:
Ca(OH)2 –Wasser-> Ca+ + 2OH–
Im Vergleich zur Natron- und Kalilaugen ist Kalkwasser eine mittelstarke Lauge.
Verwendung fand Kalkwasser beispielsweise in der Denkmalpflege. Dort nahm man an, dass mithilfe von Kalkwasser morbide Natursteine oder Putzmörtel gefestigt werden könnten. Inzwischen ist es allerdings wissenschaftlich bewiesen, dass kein Festigkeitszuwachs stattfindet und falls doch, dass dieser auf eine Umlagerung von noch im Mörtel vorhandenem Calciumhydroxid zurückzuführen ist.
Ein weiteres Einsatzgebiet des Kalkwassers ist als Sperrflüssigkeit.
Kalkwasser kann darüber hinaus als Nachweis von Kohlenstoffdioxid verwendet werden. Dieses erzeugt nämlich beim Einleiten in Kalkwasser eine weiße Trübung. Dabei entsteht erst Kohlensäure (zerfällt in Wasser sofort und reagiert mit Calciumhydroxid) und anschließend Calciumcarbonat, das als Feststoff ausfällt und deshalb die Trübung des Wassers hervorruft.
CO2+H2O -> H2CO3
H2CO3+Ca(OH)2 -> CaCO3+2H2O
Ammoniakwasser
Das Ammoniakwasser (auch Ammoniaklösung oder Salmiakgeist genannt) entsteht beim Lösen des Gases Ammoniak in Wasser:
NH3 + H2O -> NH4+ + OH–
Wie man an der Reaktionsgleichung sieht, entstehen Ammoniumionen NH4+ und Hydroxidionen OH–
Das Ammoniakwasser kann Fette lösen und und organische Substanzen aufquellen. Es ist daher ein Hausmittel zur Reinigung von Oberflächen. Auch zur Abwehr von Wespen kann Salmiakgeist verwendet werden. In der Nahrungsmittelindustrie wird Ammoniakwasser für die Produktion von Nahrungsmitteln wie Hefen und Vitaminen benötigt.
Eigenschaften von Laugen
Nahezu alle Laugen besitzen gemeinsame Eigenschaften die sie auszeichnen. Dies sind unter anderem:
- Charakteristische Färbung mit Indikatoren (z.B. Blaufärbung von Lackmus)
- Fühlen sich auf der Haut glitschig/seifig an
- Lösungen sind ätzend
- Zeigen elektrische Leitfähigkeit
- PH-Wert der Laugen liegt oberhalb des Neutralpunkts 7
- Laugen lassen sich mit Säuren neutralisieren
- Sie haben eine -OH Gruppe (Hydroxid)
Bildung von Laugen
Laugen können über verschiedene Wege gebildet werden. So entstehen beispielsweise Laugen beim Lösen von wasserlöslichen Metalloxiden im Wasser:
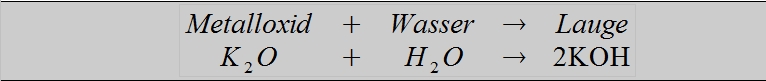
Außerdem können Laugen gebildet werden, wenn die unedlen Metalle Natrium, Kalium und Calcium direkt mit Wasser reagieren:
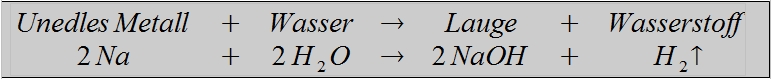
Hervorgerufen wird die Laugenwirkung, die für alle Laugen gilt (z.B. Blaufärbung von Lackmus), durch die OH-Gruppe, die alle Hydroxide enthalten. Diese Laugenwirkung entfaltet sich aber erst bei der Lösung der Metallhydroxide in Wasser. Dabei zerfallen die Metallhydroxide in Metall-Kationen und Hydroxid-Anionen, diesen Vorgang nennt man Dissoziation:
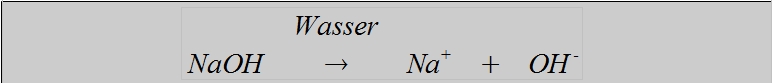
Beispielexperimente
Viele Laugen im Alltag können durch Experimente, die auch im Schulunterricht möglich sind, nachvollzogen werden. Von der Herstellung einer Lauge bis hin zum Nachweis von Laugen über einen Indikator ist alles möglich. Und auch darüber hinaus bieten Laugen eine Vielzahl an Anwendungsmöglichkeiten. Nachfolgend sollen zwei Experimente zu Anwendungen von Laugen beschrieben werden, auf die wir auch im Alltag häufig treffen.
Herstellung von Seife
Die Seife blickt auf eine lange Geschichte zurück. Schon im 3 Jahrhundert vor Chr. benutzten die Sumerer Seifen, in der Mitte des 18 Jahrhunderts wurde Seife sogar schon industriell hergestellt.
Trotz der maschinellen Herstellung von Seife seit einer langen Zeit, macht es auch noch heute Sinn, Seife selbst herzustellen. Grund dafür ist, dass bei industriell-hergestellter Seife meist unterschiedliche Zusatzstoffe verwendet werden, die die Haut reizen und zu gesundheitliche Probleme, z.B. Allergien, führen können. Bei der eigenen Herstellung von Seife kann man die Inhaltsstoffe hingegen selbst festlegen.
Eine Seife entsteht durch den Prozess der Verseifung (wird auch basische Hydrolyse genannt) aus Carbonsäureester, d.h. aus Öl oder Fett zusammen mit einer Lauge. Je nach dem was man für eine Seife herstellen möchte, verwendet man die entsprechende Lauge. Für Kern- oder Leimseife greift man auf Natronlauge zurück. Soll es eine Schmierseife werden, nutzt man Kalilauge.
Die Herstellung der eigenen Seife ist ganz einfach: Man erhitzt das Öl/Fett und gibt anschließend die Lauge mit in den Topf. Nun muss gerührt werden, bis sich Fett und Lauge vermischt haben. Die Masse wird immer dicker bis zu einem Punkt, an dem man sie in eine vorbereitete Seifenform gießen kann. Dort muss sie nun abkühlen. Diese Zeit nennt man auch „reifen“, da dort der Verseifungsprozess läuft (d.h. der Laugenanteil wird geringer und damit sinkt der pH-Wert der Seife zwischen 8,5 und 10) . Nach circa 24 Stunden kann man die Seife aus der Form nehmen und noch einmal für 3 bis 6 Wochen zum Trocken aufstellen. Auch hier ereignet sich weiter der Verseifungsprozess und die Seife wird etwas milder.
Mit Kräutern und Ölen kann man jederzeit unterschiedliche Seife herstellen.
Herstellung von Laugen-Gebäck
Das Herstellen von Laugen-Gebäck ist einfacher als man denkt. Als Grundbasis dient der Teig-Rohling, der z.B. aus einem Hefeteig besteht. Dieser Teigrohling, z.B. ein Brötchen oder eine Brezel, wird in ein Laugebad für circa 30 Sekunden gelegt und anschließend gebacken. Alternativ ist es auch möglich das Gebäck mit der Lauge einzupinseln, allerdings kann es hier passieren, dass es nach dem Backen zu Flecken kommen kann.
Das Laugebad besteht aus einer 3-4% NaOH Lösung. Diese Verdünnung der Natronlauge ist notwendig, da die Lauge im rohen Zustand sehr ungesund ist und zu Verätzungen führen kann. Das Laugebad kann durch eine Natriumhydroxidlösung (meist 33%ige Konzentration) oder auch durch NaOH-Plätzchen selbst verdünnt werden. Dafür gibt man die die Hydroxidlösung bzw. das Plätzen in soviel Wasser, bis man die entsprechende Konzentration von 3% bis 4% erreicht hat. Während dem Auflösen der Plätzen erwärmt sich das Wasser, eine exotherme Reaktion findet statt.
Doch was passiert mit der Natronlauge während des Backens im Ofen?
Durch die Wärmeeinwirkung reagiert das Natriumhydroxid auf der Oberfläche des Gebäcks mit Kohlendioxid aus der Luft zu Natron (Natriumhydrogencarbonat):
NaOH + CO2 -> NaHCO3
Auch wenn sich auf dem Gebäck noch Spuren vom Natriumhydroxid befinden ist dies kein Problem, da es mit der Magensäure (HCl) zu Kochsalz und Wasser reagiert :
NaOH + HCl -> NaCL + H2O
Charakteristische Geschmack und Farbe
Den bekannten Geschmack und die prägende Farbe eines Laugengebäcks erhält der Teigling durch die Maillard-Reaktion. Die im Teig enthaltene Stärke und Eiweiß werden in kürzester Zeit durch die Natronlauge abgebaut (z.B. Stärke in Dextrine und Einfachzucker, Eiweißstoffe werden aufgespalten z.B. in Aminosäure). Diese Stärke- und Eiweißstoffe reagieren dann wiederum in der Backhitze und führen zur Bildung von neuen Stoffen, den Melanoidinen. Diese Melanoidinen sind für den bekannten Geschmack und für die vertraute Farbe von Laugengebäck verantwortlich.